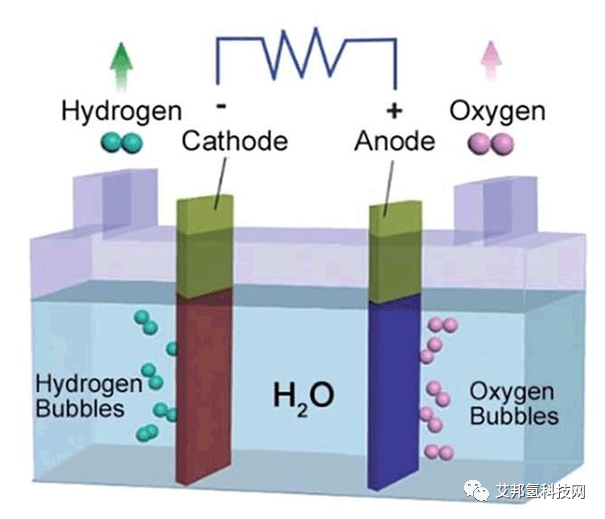
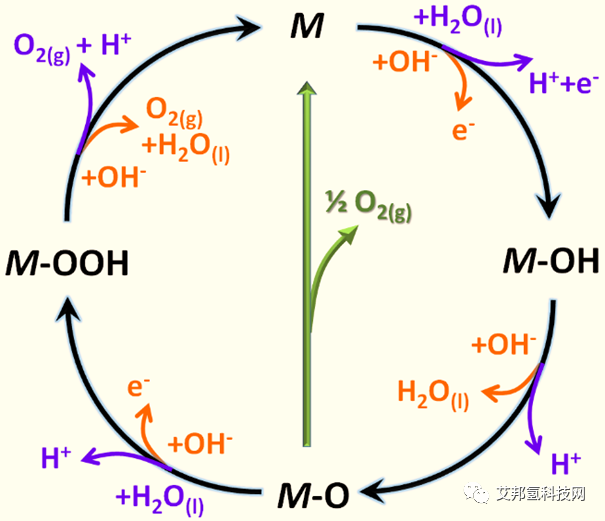
1.析氧反应(OER)
- H2O + * → OHads+ H+ + e-
- OHads→ Oads + H+ + e-
- Oads+ H2O → OOHads + H++ e-
- OOHads→ O2ads + H+ + e-
- O2ads→ O2 + *
- Overall: 2H2O→ 4H+ + O2+ 4e-
- OH-+ * → OHads + e-
- OHads+ OH- → Oads + H2O + e-
- Oads+ OH- → OOHads + e-
- OOHads+ OH-→ O2ads + H2O + e-
- O2ads→ O2 + *
- Overall: 4OH-→ 2H2O + O2 + 4e-
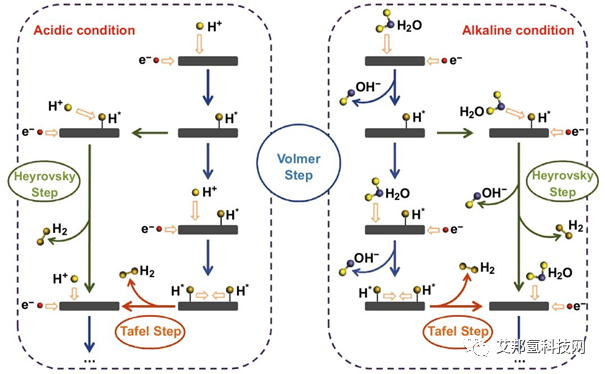
2.阴极析氢反应(HER)
-
H2O + e-→ OH- + Hads (Volmer)
-
Hads+ H2O + e- → OH- +H2 (Heyrovsky)
-
or 2Hads → H2 (Tafel)
-
H++e- + * → Hads (Volmer)
-
Hads + H++ e- → H2 (Heyrovsky)
- or 2Hads → H2 (Tafel)
原文始发于微信公众号(艾邦氢科技网):电解水制氢原理:析氧反应(OER)和析氢反应(HER)
大家好,艾邦氢能源技术网的微信公众号已经开通,主要分享氢燃料电池堆(双极板,质子膜,扩散层,密封胶,催化剂等),制氢,加氢,氢燃料汽车动力系统等相关的设备,材料,配件,加工工艺的知识。同时分享相关企业信息。欢迎大家识别二维码,并通过公众号二维码加入微信群和通讯录。


